條文本
摘要
簡介妊娠期細菌性陰道病(BV)和陰道菌群破壞與自發性早產(SPTB)風險增加相關,但妊娠期BV治療的臨床試驗顯示收效甚微或無益處。另一種假設是,懷孕前後存在的陰道細菌可能會破壞宮頸粘液的保護作用,在胎兒膜發育之前就在子宮內膜表麵定植,並導致蛻膜、胎盤和胎兒膜的低水平炎症,從而導致SPTB。本方案描述了一項針對這一假設的前瞻性病例隊列研究。
和分析方法對有意生育的艾滋病毒血清陰性的肯尼亞婦女從孕前到懷孕、分娩和產後早期進行跟蹤。參與者在受孕前每月提供陰道標本,用於陰道菌群評估。預計的分娩日期是由最後的月經周期和前三個月的產科超聲決定的。分娩後,從胎膜間采集棉簽。采集胎盤和臍帶樣本進行組織病理學檢查。廣泛的16S rRNA基因PCR和懷孕前陰道標本的深度測序將評估SPTB婦女與足月分娩婦女的物種豐富度和多樣性。用定量PCR (qPCR)比較關鍵細菌種類的濃度。Taxon-directed qPCR還將用於定量從胎膜樣本中提取的細菌,並評估細菌濃度與胎膜、胎盤和臍帶炎症的組織病理學證據之間的關係。
道德和傳播這項研究得到了肯雅塔國立醫院和華盛頓大學倫理委員會的批準。研究結果將分發給研究地點和合作機構的臨床醫生,在會議上發表,並發表在同行評審的期刊上。本研究的發現可以通過關注懷孕前陰道菌群作為SPTB的中介因素來改變思考陰道菌群和早產之間的聯係機製的範式。
- 流行病學
- 產科
- 微生物學
這是一篇開放獲取的文章,按照創作共用署名非商業性(CC BY-NC 4.0)許可發布,該許可允許其他人以非商業性的方式發布、混編、改編、構建本作品,並以不同的條款授權他們的衍生作品,前提是原創作品被正確引用,給予適當的榮譽,任何更改都被注明,且使用是非商業性的。看到的:http://creativecommons.org/licenses/by-nc/4.0/.
來自Altmetric.com的統計
本研究的優勢和局限性
這項前瞻性病例隊列研究招募了有生育意圖的肯尼亞婦女,以便從孕前到懷孕和產後早期進行隨訪和暴露測量。
在孕前期間每月收集標本,以便對接近受孕時間的陰道菌群進行檢查。
分娩時收集胎兒膜拭子和胎盤樣本,以便評估胎兒膜中細菌的檢測和濃度、炎症和早產之間的聯係。
廣泛的16S rRNA基因PCR與下一代測序和定量PCR的結合提供了陰道分泌物和胎兒膜中細菌的相對和絕對數量。
因為這是一項觀察性研究,它不能確定陰道細菌和早產之間的因果關係。
簡介
在全球範圍內,大約10%的出生是早產(妊娠<37周),但在資源匱乏的國家,這一患病率可高達18%。1早產及其後遺症是5歲以下兒童死亡的主要原因。2大多數早產是自發性早產(SPTB)。3.SPTB的病因通常未知,但高達40%可能與宮內感染有關。3 4其他風險因素包括其他感染(尿路感染、性傳播感染和全身感染)、社會人口特征(年齡、種族和教育)、3.身體質量指數的極端5牙周疾病,6解釋間隔<6個月、有SPTB病史、壓力、抑鬱和吸煙。3.對原因的進一步闡明可能為減少SPTB提供新的方法。
細菌性陰道病(BV)是一種常見的陰道疾病,其特征是從最佳狀態轉移乳酸菌-主導的陰道菌群,以高濃度的各種厭氧物種為特征。7大量研究表明,懷孕期間的BV與SPTB的風險增加有關。8然而,一項臨床試驗的meta分析得出結論,雖然妊娠20周前的抗生素治療成功地治療了BV,但SPTB的風險並沒有顯著降低。9
分子微生物學改變了對陰道菌群的認識,使其具有從低多樣性到更廣泛的表型譜乳酸菌,以細菌群落為主導的高多樣性bv相關群落的異質群。10 11探索陰道菌群和SPTB之間關係的研究得出了相互矛盾的結果。一些人發現了物種多樣性增加和早產之間的顯著關聯,12日至16日而其他人則沒有。17日至19日此外,一些研究發現,女性的相對豐度較低乳酸菌bv相關類群的物種和相對豐度較高的物種可能具有較高的早產風險。16 - 22其他研究發現陰道細菌群落類型與早產之間沒有關聯。12 14日17檢測到和濃度較高的特定陰道細菌也與早產有關,包括纖毛菌屬/ Sneathia,16日23bv相關菌1 (BVAB1)16日23Megasphaera,23加德納菌屬鞘突,24日25日Atopobium陰道,24TM7-H116和一些普氏菌物種。16
一個新的假設可以解釋懷孕期間BV治療對SPTB風險缺乏成功的原因,即孕前陰道菌群可能是比懷孕期間陰道菌群更重要的SPTB風險因素。懷孕前後出現的陰道細菌可能會破壞宮頸粘液的保護作用,26在胚胎著床前進入子宮內膜,形成宮頸粘液塞和胎兒膜的發育。這些細菌可以在蛻膜、胎盤、胎膜或羊膜腔內定植並引起慢性、低水平炎症。27 28在這種情況下,懷孕期間的抗生素治療可能來不及影響與宮內細菌相關的婦女患SPTB的風險。
微生物區係和早產研究(MPTB)招募了試圖懷孕的艾滋病毒陰性肯尼亞婦女進行前瞻性病例隊列研究,以實現以下目標:
利用寬範圍16S rRNA基因PCR和下一代測序技術,比較SPTB婦女和足月分娩婦女接近受孕時陰道菌群的物種多樣性和豐富度。
比較所選細菌屬/種的存在和濃度(基於已發表的數據)23目的1)的結果使用靶向定量PCR (qPCR)的陰道標本采樣接近受孕時間的SPTB婦女和足月分娩。
對從胎膜采集的樣品進行物種特異性qPCR分析,並對胎膜和臍帶進行組織學檢查,以確定陰道細菌是否上升到上生殖道,並引起胎膜和臍帶炎症。
和分析方法
研究設計,設定和時間
MPTB研究是一項前瞻性病例隊列研究。符合條件的婦女在懷孕前登記,並在孕前、懷孕、分娩和產後早期進行跟蹤。如統計分析部分所述,參與者將被選入病例隊列樣本。研究地點位於內羅畢的肯雅塔國立醫院、蒙巴薩的甘約尼衛生中心和海岸省總醫院。
內羅畢和蒙巴薩分別於2017年4月和2018年4月開始招生。參與者的孕前登記將持續到大約2019年6月,最後一次研究交付將在2021年進行,大約在最後一次登記18個月後。
資格標準及招聘
目標人口是目前計劃懷孕的艾滋病毒陰性婦女。其他入選標準包括:年齡≤45歲,前3個月有月經,或近期停用閉經避孕方法(如植入物、宮內激素節育器),願意遵守研究程序,並能夠提供知情同意。根據肯尼亞法律,14-17歲的未成年人有資格獲得自由。排除標準包括當前懷孕、為預防艾滋病毒/性傳播感染(STI)而使用避孕套以外的其他避孕措施、在過去3個月內注射過醋酸甲羥孕酮(DMPA)、有過宮頸或子宮手術史(剖宮產除外)、已知的自身免疫性疾病、在過去4周內使用過抗生素以及有不孕求醫史。對於已知有艾滋病毒陽性男性伴侶的女性,其伴侶必須有檢測不到的艾滋病毒載量,或者參與者必須采取接觸前預防措施。
參加者由研究人員招募,或由提供生殖或產婦保健服務地點的保健提供者轉診。以懷孕為目的而停止避孕的婦女是主要的招募人群。
研究訪問和程序
參與研究分為六個階段,包括篩檢/報名、牙周檢查、孕前、懷孕、分娩和產後(圖1).標本采集、實驗室檢測和其他臨床程序總結於表1.
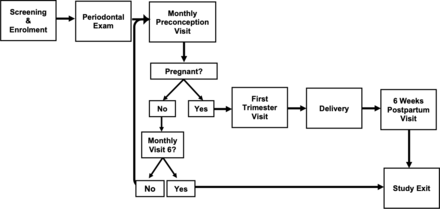
微生物群與早產研究階段-額外的參與者途徑:(1)在研究報名6個月內停用DMPA注射避孕的參與者有資格進行9個月的孕前隨訪。(2)流產的參與者有資格重新進入孕前隨訪,進行第二次妊娠嚐試。DMPA,得寶甲羥孕酮。
篩查和注冊表示“狀態”
在獲得書麵知情同意進行篩查後,研究人員根據肯尼亞指南進行尿妊娠檢測和快速艾滋病毒檢測,29並進行資格麵試。符合條件的婦女可在征得同意後立即登記。如果報名日期較晚,則需要重複進行妊娠測試,以再次確認資格。
參與者完成了一項結構化的麵對麵訪談,內容涉及人口統計、性行為、藥物使用、抑鬱症狀(患者健康問卷-9)以及生殖和病史。臨床醫生進行體格檢查和鏡下輔助盆腔檢查。如果女性處於月經期,檢查就會推遲,以避免在這段時間內采樣,因為陰道菌群會發生快速變化。30 31用推推式滌綸棉簽(FitzCo)在陰道外側壁旋轉三次,收集兩份陰道液體標本;這些被儲存起來用於陰道菌群和炎症反應評估。收集額外的生殖器標本用於性傳播感染診斷淋病奈瑟菌,沙眼衣原體而且陰道毛滴蟲通過核酸擴增試驗(NAAT),陰道和宮頸革蘭氏染色,檢測前列腺特異性抗原(PSA)和唾液酸酶升高,使用BV的護理點診斷試驗(診斷BVBLUE, Gryphus診斷)。陰道標本接種到Rogosa瓊脂上進行檢測乳酸菌.根據包括陰道分泌物在內的生殖器綜合征的指示提供綜合征管理。32根據STI NAAT結果在第一次孕前就診時提供額外治療。
檢查結束後,婦女將接受關於孕前和懷孕期間健康行為的谘詢,包括戒煙、不洗陰道和健康飲食。研究臨床醫生討論參與者的月經周期,並使用基於日曆的方法確定可能的生育窗口。排卵估計發生在下一個預期月經的第一天的14天前,排卵最多的日子強調為排卵前5天和排卵當天。33所有參與者都接受產前維生素。
牙周考試暗殺行動
牙周炎與SPTB有關6因此,參與者要接受牙周檢查。因為懷孕會增加牙齦炎症,34考試在入學後4周內進行。口腔檢查包括牙周炎的評估,使用牙周袋深度和臨床附著測量,以及蛀牙缺失填補指數和牙齦指數評估。35牙周炎的存在和嚴重程度定義使用2007年疾病控製和預防中心/美國牙周病學會的病例定義。36參與者還需完成修訂版的世衛組織口腔健康問卷。35
每月偏見訪問
在試圖懷孕期間,參與者每隔1個月返回一次研究訪問。人事保留人員在每次預約前都會給參與者打電話。進行有組織的麵談,以更新性行為和病史。女性自我收集陰道拭子用於微生物區係和炎症反應分析,陰道革蘭氏染色,PSA檢測,乳酸菌培養和唾液酸酶檢測。有生殖器症狀的參與者接受綜合征治療。32
進行尿妊娠試驗,試驗結果呈陽性的參與者將在妊娠9至12周期間進行妊娠前三個月的檢查。大多數6個月後仍未懷孕的婦女退出研究;在報名前不到6個月停用DMPA的人,由於停用DMPA後恢複生育的時間延遲,有9個月的孕前“試孕時間”。37 38
前三個月隨訪(9- - - - - -孕12周)
在妊娠前三個月就診時,進行結構化麵談,以更新性行為和病史方麵的信息。婦女自行收集陰道拭子進行菌群和炎症反應分析,陰道革蘭氏染色,PSA檢測和乳酸菌文化。然後,孕婦接受產科超聲檢查以確定孕齡。超聲由內羅畢KNH的超聲技師和蒙巴薩的一家私人放射科設施進行(培訓和質量控製見表2).美國婦產科醫生學會2014年指南用於估計胎齡,如果超聲估計的值與16周前7天最後一次月經周期計算的值不同。39如果隨後獲得了超聲檢查,如果16 - 22周與上次月經日期不同>10天,22 - 28周>14天,28周後>21天,則使用超聲檢查日期。
懷孕的參與者被推薦進行常規產前護理(ANC),並登記參加一個短信服務(SMS)項目,以支持保留(見妊娠期間保留部分)。定期收集的產前數據(如梅毒檢測結果、血壓)摘錄自參與者的ANC設施記錄和向所有肯尼亞孕婦提供的《母嬰健康手冊》。
如果參與者遭遇流產,妊娠損失的處理由非研究臨床醫生根據護理標準進行。妊娠<20周流產的婦女如果想再次懷孕,可以繼續參與研究,每月進行6次額外的孕前檢查。
保留在懷孕期間
為了提高留存率,參與者可以報名參加一個雙向短信項目的改編版,該項目最初是為支持懷孕和產後的艾滋病毒陽性肯尼亞婦女而設計的。40懷孕16周、20周和24周時發送信息,從28周開始每兩周發送一次,從產後38周到6周每周發送一次。此外,研究護士從第35周開始每周給參與者打電話,以確認妊娠狀態和計劃分娩地點。參與者被要求在分娩開始時打電話,以便研究人員能夠協調為在國家醫院或CPGH分娩收集分娩樣本,並協助確定在其他地方分娩的分娩日期。
交付過程
分娩遵循標準的產科程序,不由研究人員進行。從胎膜和胎盤樣本之間采集棉簽,由訓練有素的分娩和接生護士(培訓和質量控製描述在KNH和CPGH表2).在陰道或剖腹產時,胎盤被放置在無菌容器中。在交貨後2小時內盡快收集樣品。使用無菌技術,一對護士從羊膜和絨毛膜之間收集樣本。41從膜之間收集無菌推脫棉簽(FitzCo),放置在低溫容器中,並暫時保存在- 4℃(內羅畢)或- 20℃(蒙巴薩)冷凍室中。胎盤置於10%的中性緩衝福爾馬林中。實驗室工作人員在一個工作日內將胎兒膜拭子運送到KNH和CPGH研究實驗室的- 80°C冰箱中。實驗室工作人員還收集胎盤樣本進行組織病理學檢查。這些包括從胎膜破裂邊緣到胎盤盤邊緣的4厘米胎兒膜卷,從胎盤盤3厘米開始的1厘米臍帶切片,以及緊鄰臍帶插入位置的1厘米胎盤塊,其上覆膜。所有病理標本均保存在10%中性緩衝福爾馬林中。
研究人員從分娩記錄中提取數據,包括分娩類型(如陰道或剖宮產;辛苦的或不辛苦的;自然分娩或引產)、並發症、活產或死產以及出生體重。
產後訪問
在產後6周隨訪中,臨床醫生提取之前沒有從參與者的分娩出院報告和母嬰健康手冊中捕獲的任何ANC和分娩細節。參與者完成了關於嬰兒健康和免疫狀況的采訪。
激勵
參與者在每次研究訪問中獲得300 KSH300(約3.00美元)。這一數額與在肯尼亞進行的其他研究一致,用於支付運輸費用。懷孕的婦女可以接受免費的產科超聲檢查。對在KNH或CPGH分娩的人提供1000 KSH1000的獎勵。
實驗室方法
顯微鏡,乳酸菌培養,性傳播感染檢測,陰道液唾液酸酶和PSA檢測
陰道革蘭氏染色玻片使用Nugent和Hiller製定的標準評估BV。42檢測生理鹽水和氫氧化鉀濕坐墊是否存在活動滴蟲、線索細胞、酵母和精子。低倍掃描宮頸內革蘭氏染色切片,計數三個非相鄰油浸區的多形核白細胞並取平均值,以評估宮頸炎症。臨床醫生將陰道標本直接接種在Rogosa瓊脂上檢測可培養性乳酸菌將培養皿保存在蠟燭罐中,4小時內運到實驗室。43過氧化氫的產生是通過傳代培養乳酸菌含有辣根過氧化物酶的四甲基聯苯胺瓊脂上的分離物。44陰道標本檢測淋球菌,沙眼球菌而且t .鞘突通過NAAT (Aptima Combo-2 CT/NG檢測係統,Aptima陰道毛滴蟲分析;Hologic)。一個陰道拭子用於唾液酸酶檢測,使用市售BV診斷試驗(診斷BVBLUE;Gryphus診斷)。陰道樣本的PSA檢測是用一種市售的檢測方法(ABAcard, Abacus Diagnostics)進行的,該方法可以在無安全套性交後的24-48小時內檢測精液。45
陰道和胎兒膜樣品中細菌的分子鑒定方法
儲存的用於細菌PCR的陰道和胎兒膜拭子將用幹冰運輸到位於美國華盛頓州西雅圖的Fred Hutchinson癌症研究中心的Fredricks實驗室。Qiagen QIAamp生物菌血症DNA分離試劑盒(Qiagen, Germantown, Maryland, USA)將用於從陰道拭子中提取DNA。該方案使用珠打和朝性裂解分離細菌細胞,並回收不含PCR抑製劑的DNA。未接觸人體表麵的棉簽將被並行處理,作為假DNA提取(陰性)對照。提取的DNA將使用引物進行寬範圍的16S rRNA基因PCR,引物與小亞基rRNA基因的高度保守區域退火,擴增一個470堿基對片段,其中包含一個高度可變的序列,對物種鑒定有用。條形碼引物將用於多重樣品。4616S rRNA基因擴增子文庫將混合在Illumina MiSeq平台上,使用300 bp對端讀取進行測序。收集的數據將使用核酸條形碼歸類到單個研究樣本中。每個樣本將產生大約10,000 - 30,000個序列讀取,提供對少數物種的可靠檢測。原始序列讀取將使用Illumina的板載bcl2fastq轉換軟件V.1.8.4進行多路複用,正向和反向索引均為零錯配。DADA2軟件包將用於質量控製、過濾、對和聚類放大器序列讀取。47使用係統發育定位工具pplacer對序列變異進行分類48還有定製的陰道參考套裝。11偽提取控製也將並行處理,以排除試劑的細菌汙染。還將進行細菌特異性qPCR檢測。這項研究的重點是假設與SPTB風險增加有關的物種,如BVAB1,Megasphaera,而且Sneathia.最終測試的種/屬集將在Aim 1的深度測序數據分析後進行微調,並根據SPTB患者和非SPTB患者中單個類群的相對豐度比較選擇額外的細菌。標準外源性水母qPCR擴增對照將用於評估PCR抑製劑。49采用寬範圍細菌16S rRNA基因qPCR法測定每個樣品中的細菌總載量。
胎膜、胎盤和臍帶樣本的組織病理學檢查
胎兒膜卷、胎盤樣本和臍帶切片的H&E染色將根據有經驗的病理學家(KM)公布的指南進行分級。50急性和亞急性炎症病變將對母體和胎兒成分進行分級和分期。慢性炎症病變的特征包括觀察到慢性蛻膜炎或蛻膜漿細胞的存在。
統計分析
樣本量估計和病例隊列人群生成
目的2需要最大的樣本量,並用於指導本病例隊列研究的樣本量估計。51前瞻性病例隊列分析集將包括3名足月分娩的婦女,每名婦女都患有SPTB。假設有三個感興趣的主要種/屬,Simes的方法被用來確定經過三次試驗調整的1型錯誤率。5280例SPTB和240例足月分娩的樣本>假設,與足月分娩相比,在SPTB婦女中檢測到孕前陰道細菌種類/屬的幾率有≥2.8倍的統計學顯著差異的概率為80%>在足月分娩的孕前檢查中,該有機體的患病率為10%。
為了收集80例SPTB病例,包括自發性早產或早產性胎膜早破的婦女,大約1100名婦女將被納入隊列。一旦發生80例SPTB病例,將確定病例隊列的樣本。首先,將自然流產(妊娠<20周)和無自然分娩或胎膜早破的早產排除在外。接下來,將從剩餘的妊娠中隨機選擇一個樣本,這樣當添加到剩餘的SPTB病例中時,病例隊列樣本的足月出生與SPTB的比率將為3:1。抽樣比例f,f用公式求解:nf + (1f)*80=320,其中n是分娩的婦女總數(病例和非病例)的數據,將用於選擇隨機樣本。最後,所有剩餘的SPTB病例將被添加到隨機樣本中,創建完整的病例隊列樣本。
統計分析計劃
目的1的目標是描述和比較懷孕前陰道物種多樣性和豐富性之間的婦女SPTB與足月分娩。所有患有SPTB的婦女和病例隊列樣本中相同數量的足月分娩婦女的隨機樣本將被包括在內。為了描述物種的總體頻率和相對豐度,將為每組生成累積秩豐度圖。53我們將使用Kolmogorov-Smirnov檢驗比較SPTB婦女和足月分娩婦女的孕前陰道細菌類群的累積分布。稀疏曲線將用於評估SPTB婦女與足月分娩婦女的物種豐富度(在97%序列相似度臨界值處定義操作分類學單位的分類單元數量)。最後,我們將評估物種多樣性(Shannon多樣性指數)54)和物種豐富度(Chao1豐富度估計器55)通過比較患SPTB婦女與足月分娩婦女之間的平均值。我們將進行邏輯回歸,以SPTB狀態作為結果,並為每個物種的物種秩豐度百分比。我們將首先確定每個變量的分數統計(以SPTB狀態作為結果),然後將變量從最大到最小的分數統計進行排序。接下來,我們將按得分統計的順序對這些數據進行logistic建模,直到在單變量logistic回歸中達到0.2的p值。這些數據將被檢驗,以細化目標2中的主要假設檢驗的目標。
對於目的2,根據文獻和目的1的結果,將選擇細菌種類/屬進行qPCR檢測,比較其在懷孕前陰道標本中的存在和濃度。這些分析將使用來自完整病例隊列樣本的數據,並將對抽樣方案進行加權處理。對於每個細菌分類單元,我們將進行未經調整的邏輯回歸來檢驗該分類單元的存在與SPTB風險之間的關係。多變量logistic回歸分析將用於確定細菌種類對SPTB風險的獨立貢獻。單變量分析(p<0.10)中與SPTB相關的物種將在處理共線性後納入多變量模型。一種手動向前逐步建立模型的方法將用於解決混雜問題。潛在的混雜因素列於表3.對於選擇用於主假設檢驗的三個物種,使用西姆斯修正進行多次比較,將認為p<0.033具有統計學意義。其他細菌類群可作為探索性分析進行評價。將進行額外的探索性分析,以調查特定細菌的孕前數量與SPTB風險之間的關係。
目的3探討在陰道孕前樣本和胎膜樣本中檢測到的細菌之間的聯係,以進一步支持上升陰道細菌在SPTB中的作用。該分析還將評估在胎兒膜中發現的細菌與蛻膜炎、絨毛膜羊膜炎和絨毛炎的組織學證據之間的聯係。該分析將使用病例隊列樣本中的婦女數據和分娩樣本。暴露是為目的2的主要假設測試的三種陰道物種的每一種的孕前檢測。結果包括在胎膜、蛻膜炎、絨毛膜羊膜炎和絨毛炎中檢測到相同的細菌種類。將使用未經調整的邏輯回歸模型估計每種暴露的ORs,並使用多變量邏輯回歸分析調整潛在的混雜因素(表3).
患者和公眾的參與
患者和公眾都沒有參與這項研究的設計。提供生殖/產婦保健服務的保健提供者和研究參與者可介紹可能符合條件的婦女參加研究。
道德和傳播
孕婦和胎兒在懷孕和分娩期間存在固有風險,但參與本觀察性研究不會增加這些風險。參與研究的風險包括與用手指進行HIV檢測、性行為敏感問題和盆腔檢查相關的不適;與艾滋病毒或性傳播感染診斷相關的壓力;還有違反機密。為了將這些風險降至最低,熟練掌握英語和斯瓦希裏語的經驗豐富的肯尼亞研究人員進行了一項強有力的同意程序。在篩查時,對篩查程序進行了解釋,並獲得書麵知情同意,表格用英語和斯瓦希裏語提供。選擇參加研究的合格女性在參加研究時要經過單獨的同意程序,包括對程序的口頭解釋和書麵知情同意。參與者被告知潛在的風險,並被告知他們可以在任何時候退出研究。通過遵循良好臨床實踐程序的數據安全,將違反保密的風險降到最低。簽署的同意書被鎖在禁區的櫃子裏。 Study identification numbers are assigned to deidentify hard copies of the case report forms, which are locked in a restricted area. Data are entered into a password-protected database using encrypted computers. Results will be disseminated to clinicians at study sites and partner institutions, presented at conferences and published in peer-reviewed journals.
討論
大多數SPTB病例都沒有已知的病因。3.妊娠期BV與SPTB的風險增加相關,但妊娠期BV治療的臨床試驗顯示,SPTB的降低微乎其微或沒有降低。9MPTB研究提出了一個假設,即在孕前期間檢測到的陰道菌群可能與SPTB有關。這一發現可能會改變思考陰道菌群和早產之間聯係的機製的範式,並可用於指導旨在通過在懷孕前識別和根除高危陰道細菌來降低SPTB風險的幹預措施的開發和評估。56-58
致謝
我們要感謝內羅畢、蒙巴薩和西雅圖的診所、實驗室和行政研究人員的奉獻精神和團隊合作。我們也感謝肯雅塔國立醫院、海岸省總醫院和蒙巴薩縣衛生部支持這項研究並提供臨床和實驗室空間。我們感謝研究參與者的承諾,他們的承諾使這項議定書的持續實施成為可能。超聲波質量保證措施的製定和實施得到了Robert Nathan博士(華盛頓大學)和Christine Mamai博士(肯雅塔國立醫院)的慷慨和巧妙支持。最後,作者感謝Anne Pulei醫生、Lydia Okutoyi醫生、Raheli Mukhwana和Grace Wang 'ombe(肯雅塔國立醫院)、Charity Muthoni和Josephine Mwangi(海岸省總醫院)以及肯尼亞國立醫院和CPGH的分娩和接生護士,感謝他們為分娩樣本收集的成功培訓、監督和實施做出的貢獻。
參考文獻
腳注
貢獻者RSM是主要調查者。RSM和DNF產生了這項研究的想法,並監督研究方案的開發和實施。GJ-S為在肯尼亞征聘和保留孕婦和產後婦女的議定書的基本內容作出了貢獻。JK和WJ擔任現場首席調查員,監督肯雅塔國立醫院和甘約尼健康中心的研究人員和實施情況。EML, SL, EF, KM, AK和HA參與設計研究,協議,數據收集工具和員工培訓。BAR、RSM、DNF和SS製定了本研究的統計分析方案。DNF, SS和KM監督實驗室方法。EML協調了研究並撰寫了初稿。所有作者審閱並批準了最終稿件。
資金這項工作得到了美國國立衛生研究院的資助(NICHD R01 HD087346-RSM)。RSM獲得了額外的指導支持(NICHD K24 HD88229)。EML由博士預科獎學金(NIAID T32 AI07140-Lukehart)支持。數據收集和管理使用REDCap電子數據捕獲工具,由華盛頓大學轉化健康科學研究所主辦,由NCATS/NIH資助(UL1 TR002319, KL2 TR002317和TL1 TR002318)。
相互競爭的利益RSM從盧平製藥公司獲得了谘詢酬金,並從Hologic公司獲得了華盛頓大學的研究資金。
病人同意發表不是必需的。
倫理批準肯雅塔國家醫院倫理和研究委員會#P70/10/2016;華盛頓大學IRB #STUDY00001472。
來源和同行評審不是委托;外部同行評議。


