條文本
摘要
背景/目標尿抗原檢測已被用於快速鑒別鏈球菌引起的肺炎肺炎患者的感染,從而導致比使用傳統診斷培養方法更早的靶向治療。本研究旨在更新有關泌尿係抗原檢測的診斷準確性的知識肺炎鏈球菌對疑似肺炎的急性呼吸衰竭患者進行係統回顧和薈萃分析。
方法使用MEDLINE和Cochrane中央對照試驗登記冊對截至2020年6月3日發表的研究進行了係統檢索。選擇和分析了臨床診斷為肺炎的成人患者中尿抗原檢測與培養或塗片診斷方法的診斷效果的前瞻性和回顧性隊列研究(英文)。使用QUADAS-2工具評估偏倚風險,並應用雙變量隨機效應模型對所選研究進行meta分析。
結果共篩選2179項研究,其中30項符合質量評估和薈萃分析的合格標準。總的來說,來自12 366例患者的數據,包括1548例(12.5%)目標條件和疑似肺炎球菌肺炎的患者,納入了分析。納入研究的總體質量被認為是嚴重的。計算的合並敏感性和特異性分別為0.66 (95% CI 0.62 ~ 0.69)和0.90 (95% CI 0.85 ~ 0.93)。
結論尿抗原檢測對於明確診斷肺炎鏈球菌肺炎患者的感染。
- 傳染病
- 診斷微生物學
- 內科醫學
- 微生物學
數據可用性聲明
所有與研究相關的數據都包含在文章中或作為在線補充信息上傳。不適用。
這是一篇開放獲取的文章,按照創作共用署名非商業性(CC BY-NC 4.0)許可發布,該許可允許其他人以非商業性的方式發布、混編、改編、構建本作品,並以不同的條款授權他們的衍生作品,前提是原創作品被正確引用,給予適當的榮譽,任何更改都被注明,且使用是非商業性的。看到的:http://creativecommons.org/licenses/by-nc/4.0/.
來自Altmetric.com的統計
本研究的優勢和局限性
該方案提前注冊,並根據係統評審和薈萃分析首選報告項目提交。
采用Cochrane手冊推薦的統計分析方法和偏倚風險評估工具。
以英文以外的語言報告的論文沒有列入,而且沒有使用Embase數據庫和Grey文獻作為數據源,這可能導致相關論文丟失或發表偏倚。
簡介
鏈球菌引起的肺炎是成人社區獲得性肺炎最常見的原因,也是肺炎引起急性呼吸衰竭的主要原因。1肺炎球菌性肺炎的死亡率因發病時疾病的嚴重程度和宿主因素而異,但在伴有菌血症時,90天死亡率非常高,約為25%-30%。2
肺炎球菌性肺炎的診斷通常通過鑒別確診肺炎鏈球菌或在血液樣本或呼吸道樣本(如痰液或胸膜液)的培養中檢測。革蘭氏染色快速但不高敏感性/特異性。3.培養試驗需要幾天才能得到結果。因此,很多肺炎病例都是靠經驗治療的。經驗性治療通常是有用的,因為它考慮到病原體的知識,包括基於當地高質量監測係統的耐藥性/易感性、患者的危險因素和共病以及症狀的嚴重程度。然而,並不是每個國家、地區或醫院都有高質量的監測係統,即使有,如果尿抗原檢測就能快速診斷肺炎鏈球菌感染時,可選擇一種更特定的抗菌劑。因此,我們相信這可能有助於降低由耐藥細菌和抗生素相關細菌引起的個人感染風險艱難梭狀芽胞杆菌感染。4個5
BinaxNOW鏈球菌引起的肺炎抗原卡(BinaxNOW-SP;Abbott, Abbott Park, Illinois, USA)是一種免疫層析檢測肺炎鏈球菌在尿液。它在世界範圍內被用作一種快速診斷方法肺炎鏈球菌肺炎患者感染,可在收集尿液後15分鍾內獲得有臨床價值的結果。2013年,以BinaxNOW-SP為指標試驗,以既定的培養或塗片方法為參考標準,對社區獲得性肺炎患者進行了兩項係統綜述和meta分析。6 7然而,隨後報道的幾項研究包含非常大的樣本量,其敏感性往往略低於之前的係統綜述,因此,我們認為有必要更新診斷準確性的證據。6 - 10因此,為了彌補這一知識差距,我們進行了一項係統回顧和meta分析,比較尿抗原檢測(UATs)與現有培養或塗片方法在診斷疑似肺炎的急性呼吸衰竭患者中的敏感性和特異性。
方法
我們對以前發表的關於診斷測試準確性(DTA)的研究進行了係統回顧和薈萃分析。我們遵循Cochrane DTA評審手冊中概述的方法學標準11並使用DTA研究係統回顧和元分析的首選報告項目12報告我們的調查結果。該評審方案在大學醫院醫學信息網絡臨床試驗注冊中心(UMIN 000041081)進行了前瞻性注冊,也可在在線補充材料.這個係統的審查不需要倫理上的批準和同意。
患者和公眾的參與
在進行這項研究的整個過程中沒有病人和公眾的參與。
種群、指標檢驗和目標條件
研究對象為疑似肺炎的急性呼吸衰竭成年患者。如果一項研究同時涉及兒童和成人,我們隻提取與成人患者相關的數據,並排除與成人患者相關的數據無法與兒童患者相區分的研究。感興趣的指數測試是UATs,如BinaxNow-SP。目標條件為參照標準方法診斷的肺炎球菌性肺炎。對於參考標準,如果痰革蘭氏染色或血液、胸膜液或呼吸道樣本(如痰液、支氣管肺泡灌洗液或其他)培養得到至少一個陽性結果,則視為陽性數據。
研究資格和選擇
選擇了所有用英文撰寫的研究,包括前瞻性、回顧性和觀察性(隊列或橫斷麵)研究,以及隨機對照試驗的二次分析。我們排除了診斷性病例對照研究(雙門研究)和缺乏DTA數據的病例研究,即真陽性(TP)、假陽性(FP)、真陰性(TN)和假陰性(FN)值。兩位作者獨立篩選每項研究的合格性並提取數據。審查員之間的分歧通過討論或第三個審查員來解決。
電子搜索
為了確定所有符合條件的研究,我們通過PubMed(於2020年6月3日訪問)和Cochrane對照試驗中央登記處(於2020年6月3日訪問)搜索了醫學文獻分析和檢索係統在線(MEDLINE)。有關搜尋策略的詳情載於在線補充文件1.開發搜索策略得到了京都立醫科大學(日本京都)醫學圖書館員的支持。
數據提取和質量評估
使用預先定義的數據提取表提取以下數據,其中包括研究特征(作者、發表年份、國家、設計、樣本量、臨床環境、利益衝突和資金來源)、患者特征(納入/排除標準、臨床和人口統計學特征)、指數檢驗(UATs)、參考標準(痰革蘭氏染色、血培養、痰培養、胸膜液培養、或培養任何其他呼吸樣本)和診斷準確性參數(TP, FP, FN和TN)。兩名研究人員使用QUADAS-2工具評估了偏見的風險,13其中包括四個偏倚風險域和三個適用性域。任何異議都通過討論或第三位審查員來解決。由於DTA研究中缺乏發表偏倚的證據,也缺乏可靠的評估方法,因此沒有對發表偏倚進行統計評估。11
統計分析和數據綜合
使用的是《Cochrane診斷測試準確性係統回顧手冊》。11在配對森林圖中捕獲95% ci的診斷敏感性和特異性估計,以評估研究異質性。我們使用二元隨機效應模型進行meta分析。隨機效應模型試圖通過假設所選研究是來自更大人群的隨機樣本,來推廣納入研究之外的發現。14所有分析均采用Review Manager V.5.3 (Cochrane Collaboration, London, UK)和STATA/SE V.16.1 (StataCorp)進行。所有統計分析均采用5%的雙麵alpha誤差進行。
非均質性評價
方案中預先規定的亞組分析用於調查以下亞組之間的敏感性和特異性是否不同:(1)參考標準的差異,(2)存在免疫功能低下的患者,(3)在進行UAT之前使用抗生素,(4)住院或門診患者,(5)使用的UAT類型。
敏感性分析
我們對QUADAS-2的所有領域進行了限製在低偏倚風險的研究的敏感性分析。
結果
共篩選2179項研究,其中30項符合合格標準,納入質量評估和meta分析。詳細的選擇方案和排除原因見圖1.
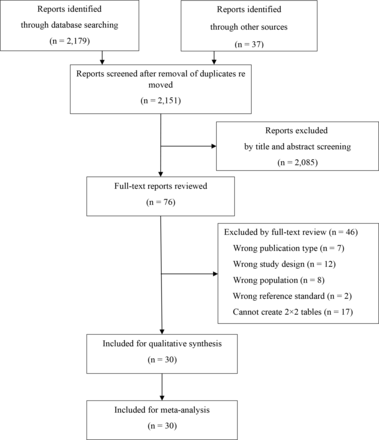
研究選擇協議(PRISMA流程圖)。PRISMA,係統回顧和薈萃分析的首選報告項目。
研究特點
從30項研究中檢索了12 366例患者的數據,其中1548例(12.5%)為肺炎球菌性肺炎。患者的中位和平均年齡為45 - 74歲,其中男性居多(51%-79%)。肺炎球菌性肺炎的中位患病率為16.7% (IQR: 9.5-22.9)。21項研究為前瞻性研究,5項研究為回顧性研究,4項研究性質不明。大多數研究都是在住院患者環境下進行的,但有三項研究包括門診患者。每個研究中使用的患者特征和參考標準總結在表1.所有研究的指標試驗均為BinaxNow-SP。參照標準由18項研究中的血液、呼吸道樣本(或塗片)或胸膜液陽性培養確定,9項研究中的血液或呼吸道樣本(或塗片)陽性培養確定,2項研究中的血液培養確定,1項研究中的呼吸道樣本培養(或塗片)確定。
偏見評估的風險
在患者選擇方麵,我們評估了10項具有高偏倚風險或高度關注適用性的研究(圖2),因為排除免疫缺陷患者是不適當的,而且當納入患者的時間框架有限時,樣本不是連續的。在指數測試中,一項研究在適用性方麵被評為高風險關注。該研究使用清晨尿液診斷肺炎球菌性肺炎;然而,它不被認為是普遍的,因此結果的適用性在其他設置和實際臨床實踐中被認為是高度關注的適用性。對於參考標準,由於參考標準不是血液培養、呼吸樣本培養(或塗片)和胸膜液培養的複合,我們評估了11項具有較高偏倚風險或高度關注適用性的研究。在患者流量評估中,我們評估了16項研究存在較高的偏倚風險,因為並非所有患者都進行了血培養作為參考標準。綜合來看,納入研究的整體質量是嚴重的。
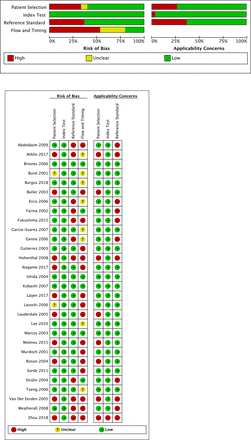
偏倚風險評估總結。使用QUADAS-2工具評估偏倚風險。QUADAS-2工具旨在評估初級診斷準確性研究的質量。綠色:低偏差風險或適用性低關注。紅色:偏倚風險高或適用性高。
薈萃分析結果
每項研究中UTAs對肺炎球菌肺炎的診斷準確性的總結在森林圖中呈現圖3.計算的合並敏感性和特異性分別為0.66 (95% CI 0.62 ~ 0.69)和0.90 (95% CI 0.85 ~ 0.93)。在目標疾病患病率為10%的1000例患者中,檢測到以下情況:TP患者66例(95% CI 62 ~ 69), FN患者34例(95% CI 31 ~ 38), TN患者810例(95% CI 765 ~ 837), FP患者90例(95% CI 63 ~ 135)。對不同流行率估計數(5%-15%)的調查結果載於在線補充文件2.
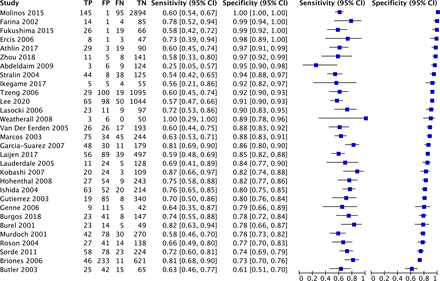
元分析中納入的研究的配對森林圖。FN,假陰性;FP,假陽性;TN,真陰性;TP,真正的積極。
亞組和敏感性分析
我們對兩個參考標準進行了亞組分析:(1)血液、呼吸道樣本(或塗片)或胸腔液培養陽性,(2)血液或呼吸道樣本培養陽性(或塗片),(3)僅血液培養陽性和(4)呼吸道樣本(或塗片)陽性(圖4一).基於17項使用參考標準A的研究表1),敏感性和特異性分別為0.69 (95% CI 0.64 ~ 0.73)和0.88 (95% CI 0.80 ~ 0.93)。基於使用參考標準B的9項研究,敏感性和特異性分別為0.59 (95% CI 0.52 ~ 0.65)和0.93 (95% CI 0.87 ~ 0.96)。我們無法對參考標準C和D進行亞組分析,因為這些診斷方法僅在少數研究中使用。
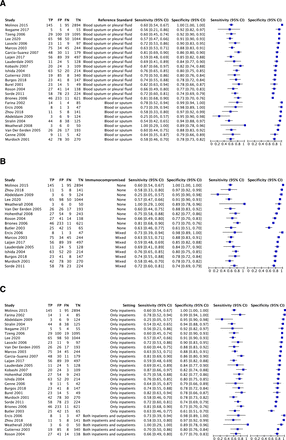
根據(A)參照標準的差異,(B)存在免疫功能低下的患者,(C)隻包括住院患者,或同時包括住院和門診患者,納入亞組分析的研究的配對森林圖。FN,假陰性;FP,假陽性;TN,真陰性;TP,真正的積極。
關於免疫功能低下患者的存在,由於沒有研究專門評估這一人群,我們在排除的免疫功能低下參與者和混合研究之間進行了亞組分析,分別為10和8項研究(圖4 b).納入組的敏感性和特異性分別為0.64 (95% CI 0.57 ~ 0.70)和0.93 (95% CI 0.78 ~ 0.97),混合組的敏感性和特異性分別為0.65 (95% CI 0.60 ~ 0.70)和0.83 (95% CI 0.79 ~ 0.87)。
關於住院患者或門診患者,由於沒有隻包含門診患者的研究,我們在隻包含住院患者的研究和同時包含住院和門診患者的研究之間進行了亞組分析(分別為23和5項研究)(圖4 c).僅住院患者研究的敏感性和特異性分別為0.66 (95% CI 0.62 ~ 0.71)和0.89 (95% CI 0.82 ~ 0.93),混合人群研究的敏感性和特異性分別為0.67 (95% CI 0.56 ~ 0.76)和0.90 (95% CI 0.79 ~ 0.96)。
由於缺乏數據,我們無法對UAT或不同類型UATs的既往抗生素是否存在進行亞組分析。也沒有進行敏感性分析,因為在QUADAS-2的所有領域中,低偏倚風險的研究數量較少。
討論
這項係統綜述和薈萃分析包括30項研究,其中彙集的敏感性和特異性分別為0.66 (95% CI 0.62 ~ 0.69)和0.90 (95% CI 0.85 ~ 0.93)。這些結果表明敏感性中等,特異性高,與以往的meta分析結果一致。5個6然而,先前的一項包括10項研究的分析報告稱,該方法具有更高的敏感性(0.75,95% CI 0.71 ~ 0.79)和特異性(0.95,95% CI 0.92 ~ 0.98)。5這一差異可能是由於排除了超過三分之一的目標人群之前使用抗生素的研究,以及排除了未知病原微生物引起的肺炎。
亞組分析顯示,由於參考標準的不同,敏感性和特異性沒有顯著變化。此外,在包括免疫功能低下患者的研究中,特異性往往較低,這表明在臨床實踐中解釋來自免疫功能低下患者的UAT結果時可能需要謹慎。此外,包括門診病人的研究結果與隻包括住院病人的研究結果相似,這表明UATs對門診病人和住院病人可能同樣有用。然而,沒有研究包括門診患者;因此,需要進一步的研究。
我們的研究優勢如下。自最近一次現有的係統綜述發表以來,已有7年多的時間,兩項調查的結果顯示出一些變化。5個6在目前的係統綜述中,我們能夠通過包括2013年以來發表的8項研究報告更新的結果,包括大樣本量的研究。其次,我們可以通過納入免疫缺陷患者來評估敏感性和特異性,這可能對臨床實踐有幫助。第三,本研究結果提示所收集的資訊可能同時適用於門診及住院病人。
盡管如此,這項研究也有一些局限性。首先,我們沒有將Embase數據庫或灰色文獻作為數據源,而隻納入了用英文描述的文章。因此,存在缺失相關研究或發表偏倚的可能性。然而,我們試圖通過手工和引文檢索提取盡可能多的相關研究。其次,根據診斷肺炎的臨床症狀和需要住院治療的嚴重程度來診斷急性呼吸衰竭。因此,一些沒有急性呼吸衰竭的肺炎患者可能被納入本研究人群。第三,兒科患者和院內肺炎患者未納入本係統綜述。這些患者的診斷準確性有待進一步研究。第四,本研究的整體質量被認為是嚴重的,主要是因為沒有收集所有參與者的血培養,但不知道每個研究中哪些參與者沒有收集血培養,這可能影響了本研究的結果。第五,雖然我們將參考標準定為痰革蘭氏染色,或血液、胸膜液或呼吸道樣本培養,在以往的文獻中可能被接受,但也有一些人認為,肺炎球菌性肺炎和其他傳染病的診斷很難確定金標準。 Recently, in a research question of diagnostic accuracy for infectious disease without widely accepted gold standard, the latent class analysis is suggested as an alternative method. We did not perform it because it was not planned in the analysis protocol; however, in further research, it may be valuable to consider the latent class analysis. Sixth, we were unable to evaluate the effect of antibiotic use, although some studies reported that 21%–70% of the participants received prior antibiotics. Fourth, all the included studies used BinaxNow-SP; thus, we could not evaluate the effect of different types of UATs. Seventh, we were not able to evaluate the effect of differences in disease severity. Nonetheless, we believe that this effect is small because the standard mechanism of the antigen test regardless of the symptoms. Eighth, previous reports have indicated that UATs inspection performance may vary from period to period, although the cause is not known.15日16本研究沒有在亞組分析中檢驗這一點,然而,未來的分析可能需要考慮由於檢驗表現的不同時期的異質性。第九,UAT不檢測抗微生物藥物敏感性/耐藥性,可能對抗微生物藥物處方沒有直接影響。即使使用UAT,也應根據當地監測係統、患者風險因素、基礎疾病和嚴重程度等對病原體的了解來選擇抗菌素。第十,最近發生肺炎球菌性肺炎的患者在發病後數周內可提供FP結果。17因此,在使用UAT時,應確定患者最近的肺炎史,並考慮到這一點來解釋。最後,UAT對肺炎球菌肺炎的診斷準確性可能在COVID-19流行期間發生了變化。在尋找納入研究時,在COVID-19暴發後沒有可用的研究,因此無法考慮COVID-19暴發的影響;UAT對COVID-19暴發後肺炎球菌肺炎的診斷準確性將在未來的研究中考慮。
綜上所述,報告的高集合特異性和中等集合敏感性表明UATs有助於排除肺炎球菌性肺炎,而不是排除它。盡管有上述局限性,我們的研究表明UATs可能對疑似肺炎患者的診斷有用。
結論
我們進行了一項係統綜述和meta分析,其中包括最近的大樣本量研究,以比較UATs作為評估疑似肺炎的急性呼吸衰竭患者的診斷工具的敏感性和特異性。我們的結果與以往的研究相似,表明UATs具有高特異性和中等敏感性。因此,UATs可用於對疑似患有肺炎的患者快速作出明確診斷。
數據可用性聲明
所有與研究相關的數據都包含在文章中或作為在線補充信息上傳。不適用。
倫理語句
病人同意發表
參考文獻
腳注
推特@YasuoShun
合作者Yasuo Shunsuke, Murata Maki, Nakagawa Natsuki, Kawasaki Takuo Yoshida, Koichi Ando, Okamori Satoshi, Okada Yohei
貢獻者所有作者都參與了研究設計。SY、MM、NN、TK、TY、KA、SO和YO確定了納入meta分析的研究並分析了數據。SY和MM起草了手稿,YO監督了手稿的起草。所有作者都參與了數據的解釋和討論。所有作者閱讀並批準了最終稿件。SY作為擔保人負責研究的整體內容。
資金作者們還沒有從任何公共、商業或非營利部門的資助機構為這項研究宣布具體的資助。
相互競爭的利益沒有宣布。
患者和公眾的參與患者和/或公眾未參與本研究的設計、實施、報告或傳播計劃。
來源和同行評審不是委托;外部同行評議。
補充材料本內容由作者提供。它沒有經過BMJ出版集團有限公司(BMJ)的審查,也可能沒有經過同行評審。討論的任何意見或建議僅僅是那些作者(s)和不被BMJ認可。BMJ放棄從放在內容上的任何依賴產生的所有責任和責任。如果內容包含任何翻譯材料,BMJ不保證翻譯的準確性和可靠性(包括但不限於當地法規、臨床指南、術語、藥品名稱和藥物劑量),並且不對翻譯和改編或其他原因引起的任何錯誤和/或遺漏負責。


