條文本
摘要
簡介低嗅覺和嗅覺喪失在COVID-19中很常見。大多數患者在4周內恢複正常嗅覺,但2個月後,大約20%的患者仍會嚴重喪失嗅覺,並可能持續一年或更長時間。這些持續的嗅覺障礙極大地影響了日常生活。有假說認為,新冠肺炎在嗅覺神經周圍和嗅覺通路引發炎症,導致嗅覺障礙。皮質類固醇可以減少這種局部炎症反應,改善氣味。
和分析方法我們將開展一項單中心、隨機、安慰劑對照試驗,以確定短期大劑量口服潑尼鬆龍治療COVID-19後早期持續嗅覺喪失的療效。根據PCR/抗原檢測陽性結果,我們將納入確診COVID-19後12周內持續(>4周)嗅覺喪失的116例患者。一組接受40毫克強的鬆龍治療10天,另一組接受對照安慰劑治療。此外,所有患者將進行為期12周的嗅覺訓練。主要結果是通過嗅棒測試來測量客觀的嗅覺功能。次要結果是通過味覺條測試的客觀味覺功能和通過三份問卷測量的主觀味覺和嗅覺能力、三叉神經感覺、生活質量和鼻腔症狀。這些結果將在治療前和12周後進行測量。
道德和傳播烏得勒支大學醫學中心機構審查委員會批準了研究方案(21-635/G-D, 2021年10月)。試驗結果將在同行評議的醫學期刊和科學會議上分享。
試驗注冊號碼NL9635。euctr2021 - 004021 - 71 -問。
- 新型冠狀病毒肺炎
- 耳鼻咽喉科
- 傳染病
這是一篇開放獲取的文章,按照創作共用署名非商業性(CC BY-NC 4.0)許可發布,該許可允許其他人以非商業性的方式發布、混編、改編、構建本作品,並以不同的條款授權他們的衍生作品,前提是原創作品被正確引用,給予適當的榮譽,任何更改都被注明,且使用是非商業性的。看到的:http://creativecommons.org/licenses/by-nc/4.0/.
來自Altmetric.com的統計
本研究的優勢和局限性
這是一項大樣本量的雙盲隨機對照試驗,以便對強的鬆龍和嗅覺訓練或僅對COVID-19後嗅覺喪失患者進行嗅覺訓練進行比較。
我們對主要結果和次要結果進行客觀測量:嗅覺和味覺功能。
除了客觀的嗅覺和味覺功能外,還將評估多種結果測量指標,如生活質量和鼻腔症狀。
考慮到長期的影響,可以考慮在6-12個月後進行額外的隨訪測量。
嗅覺障礙問卷還沒有在荷蘭COVID-19後嗅覺喪失患者中得到驗證。
背景
嗅覺能力的部分或完全喪失,分別是嗅覺減退和嗅覺喪失,是COVID-19常見的早期特征,1 2大約三分之二的病人會出現這種情況。3 4雖然絕大多數患者在4周內恢複,但大約有五分之一的患者在2個月後仍然嚴重喪失嗅覺。5嗅覺能力下降,嗅覺減退,6個月後持續10%-46%6 - 8可持續一年或更長時間,其中7%-9%為功能性嗅覺障礙。9日10除了嗅覺喪失,患者還報告味覺障礙和嗅覺改變,開始於一段時間的嗅覺缺失。11日12在嗅覺缺失症(嗅覺扭曲)中,人們感知到的氣味與平時不同,或者在幻聞症中,沒有氣味源也能感知到氣味。持續的嗅覺障礙與患者生活質量的顯著降低有關,包括抑鬱症狀的增加和營養問題。13
對於COVID-19期間和之後嗅覺障礙的病理生理學,目前還沒有明確的答案。在普通感冒病毒中,嗅覺的喪失通常是由於鼻粘膜的腫脹。然而,在SARS-CoV-2感染中沒有觀察到鼻粘膜腫脹。1 14 15據推測,SARS-CoV-2通過ACE2受體進入嗅覺上皮的支持神經細胞,從而導致嗅覺喪失。16在反應中,快速的自身免疫反應激活淋巴細胞和巨噬細胞,並導致細胞因子的釋放。這種自身免疫反應在患者之間可能有很大差異,並可能解釋長期嗅覺障礙的差異。14日17COVID-19期間的這種炎症反應也出現在某些大腦區域,如嗅覺通路。18 19
目前還沒有科學證明的covid -19後貧血或嗅覺喪失的治療方法。在其他包括嗅球在內的病毒後嗅覺喪失中,嗅覺療法是迄今為止唯一被證實有效的改善嗅覺功能的治療方法。20 21在氣味療法中,病人在3個月的時間裏每天嗅一組已知的氣味。持續的訓練將加快和增加嗅覺恢複的程度。20 21現在,氣味療法建議所有COVID-19後持續失去嗅覺的患者,22然而,這種效應本身似乎是有限的。
對於因炎症反應而導致神經功能喪失的疾病,如突然感音神經性聽力喪失或貝爾氏麻痹,給予短療程的大劑量口服皮質類固醇。23日24在這些疾病的早期階段,自身炎症作用是可逆的。最近,口服類固醇治療了新冠病毒感染後出現嗅覺喪失的患者,效果很好:兩項隨機對照試驗(rct)包括COVID-19後1個月持續嗅覺喪失的患者,結果顯示,與對照組相比,更多的患者在接受皮質類固醇治療後恢複了功能。25日- 27日盡管納入的病例數量有限,隨訪時間短,試驗設計非盲法,但臨床效果似乎很有希望。
如果潑尼鬆龍聯合氣味療法有效,就可以預防長期殘疾。因此,我們建議通過一項單中心、雙盲、安慰劑對照的隨機試驗,研究口服皮質類固醇治療聯合氣味療法的療效。
和分析方法
研究設計與設置
該研究是一項單中心、隨機、安慰劑對照臨床試驗,在荷蘭烏得勒支大學醫學中心(UMCU)耳鼻咽喉科進行。患者將被隨機分為兩組:服用強的鬆龍10天或安慰劑10天。此外,所有患者將進行為期12周的嗅覺訓練。第一次就診時,在治療開始前,患者的嗅覺和味覺功能將通過嗅棒測試(SST)和味覺條測試(TST)進行測試。主觀測量包括問卷調查。在10天的治療後,研究人員會打電話給所有患者檢查治療依從性以及是否有任何副作用。12周後,將通過SST、TST和相關問卷進行評估圖1).
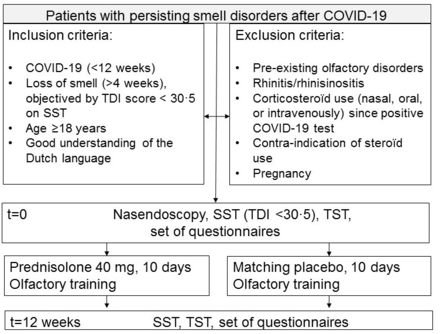
研究流程圖。SST,嗅棒測試;tdi評分、閾值、判別、識別評分;TST,味道條試驗。
患者和公眾的參與
全國患者協會參與了這項研究的實施,申請資金並招募患者。參加這項試驗的患者,如果願意,將會被告知試驗結果。
研究目標
本研究的主要目的是確定短時間大劑量口服潑尼鬆龍治療COVID-19後持續嗅覺喪失的療效。這將用客觀海表溫度來測量。次要目的是通過附加問卷調查,研究潑尼鬆龍對客觀TST測量的味覺功能和主觀嗅覺、味覺和三叉神經功能的療效,嗅覺/味覺變化對生活質量和鼻腔症狀的影響。
研究人群
116名在COVID-19診斷後12周內(根據PCR或抗原檢測)呈陽性(>或4周)持續(>4周)嗅覺喪失的患者(>18歲)將納入研究。在招聘方麵,我們會與公共衛生服務機構、耳鼻喉科診所和本地病人組織合作。預計最多需要18個月的時間,主要取決於荷蘭的感染人數。包括從11月16日開始到2月10日。隨訪結果於2月2日至5月10日進行測量。患者需符合以下條件方可參與:
入選標準
最近被診斷為COVID-19(小於12周),經荷蘭公共衛生研究所PCR或抗原陽性確認。
嗅覺持續喪失(>4周),以閾值、鑒別、識別(TDI)客觀化,SST <30.5。
年齡18歲或以上,並能給予知情同意。
良好的荷蘭語理解能力。
排除標準
預先存在的嗅覺障礙。
慢性鼻炎或鼻竇炎(伴或不伴鼻息肉)。
自COVID-19檢測呈陽性以來使用皮質類固醇(鼻、口服或靜脈注射)。
懷孕。
類固醇的禁忌症,包括:
使用藥物(皮下或口服)治療的糖尿病。
胃潰瘍、胃出血。
精神病。
正在進行的腫瘤疾病。
樣本大小
樣本量的計算基於早期試點研究的平均值和SDs。26SST評分的冪為0.90,alpha為0.05,平均差異為5.5 (SD 8.0),總樣本量為92。為了校正可能的非參數檢驗,樣本量增加了15%。由於該研究對患者的時間和精力有限,預計最大的輟學率為10%。總樣本量為116例,每組58例。
隨機、盲法和治療分配
患者將被隨機分配到兩組中的一組。負責準備治療和安慰劑藥物的藥房製作了一份分組隨機序列清單,上麵的患者受試者編號與研究藥物編號相關聯。該藥房是荷蘭最先進的良好生產實踐複合藥房,獨立於我們的部門。為了盡量減少組間的季節性影響,隨機分組為4名患者。兩組人的重量是一樣的。
對患者、醫生和結果評估人員進行盲法治療分配。
隻有在完成所有分析之後,研究人員和患者對治療分配的盲目性才會被打破。如果由於醫療原因需要進行除盲,則可以由臨床藥物研究藥房隨時進行。
幹預
A組給予強的鬆龍膠囊40 mg,每天1次,連續10天。B組給予安慰劑膠囊,每天1次,連續10天。兩組患者都將進行12周的嗅覺訓練。在這項訓練中,患者每天兩次嗅出四種氣味(玫瑰、檸檬、桉樹、丁香)。20.將通過劃掉每日時間表來監測培訓的符合性。患者在第一次就診時接受研究藥物和嗅覺訓練包。
待測結果
在納入時,將收集人口統計數據,如性別、年齡和母語。醫療狀況包括藥物使用情況、病史、感染COVID-19的日期、失去嗅覺的日期和接種疫苗的情況。在門診第一次和第二次就診時將收集結果測量值。在第一次就診時,將進行鼻內窺鏡檢查,以消除嗅覺喪失的其他原因。對於主要結局,本次隨訪期間進行SST,當測量TDI評分>30.5時,仍可能導致排除。二級結果將通過TST和問卷進行評估。此外,患者還需要填寫三份問卷:經驗證的sino - nose Outcome Test−22問卷(SNOT-22)、用視覺模擬量表(VAS)自述的嗅覺、味覺、腮腺炎、三叉感覺問卷、28以及翻譯的嗅覺障礙問卷(QoD)。29 30所有患者將進行12周的嗅覺訓練。治療開始12周後,將重複進行SST、TST和完成相同問卷的比較。主要和次要結果都將登記在電子病例報告表格(eCRF)中,即umcu認可的Castor EDC係統。
解釋考試
嗅覺功能將通過SST進行評估,SST是一種廣泛使用、驗證良好的商用測試。31SST由Burghart公司生產,這是一家醫學認證公司(ISO 13485),表明氣味及其溶劑不會對健康造成風險。該測試電池使用充滿氣味和/或溶劑的筆狀氣味裝置來檢測鼻化學感覺性能。該測試包括三個部分:檢測閾值(THR)、辨別(DIS)測試和氣味識別(ID)測試。TDI評分為THR、DIS和ID之和,取值範圍為1 ~ 48。分數越高,說明嗅覺功能越好。
THR將用含有不同濃度正丁醇的標準係列筆進行測量。在樓梯式程序中,三支筆將以隨機順序呈現給參與者。在這些筆中,一支含有氣味,兩支含有溶劑。參與者必須指出哪支筆裏有這種氣味。為了測量DIS能力,將提出16個三種氣味的三聯。三聯包含兩支氣味相同的筆和一支氣味不同的筆。參與者必須辨別哪支筆的氣味不同。在ID測試中,將呈現16支具有共同氣味的鋼筆。參與者必須從每支筆的四個描述符中選擇正確的描述符。
結核菌素:這個驗證測試使用了浸漬了不同濃度的基本口味甜、鹽、苦、酸的濾紙品嚐條。32用四種濃度的甜(0.05、0.1、0.2或0.4 g/mL蔗糖)、鹽(0.016、0.04、0.1或0.25 g/mL氯化鈉)、酸(0.05、0.09、0.165或0.3 g/mL檸檬酸)或苦(0.0004、0.0009、0.0024或0.006 g/mL鹽酸奎寧)浸漬濾紙。在把一張紙放在舌頭上後,患者被要求用五種可能的答案(甜的、酸的、鹹的、苦的或無味的)來識別味道。味覺條采用半隨機強製選擇程序呈現。由於每種味道的得分從0到4不等,所以味覺總分從0到16不等。分數越高,味覺功能越好。
解釋調查問卷
SNOT-22:該問卷由22個關於鼻腔症狀和健康相關生活質量的問題組成。患者需要用李克特5分製量表對這些症狀進行評分;分數越高,症狀越嚴重。28在慢性鼻竇炎患者中,術後8.9分的改善被認為是臨床顯著差異。33
通過VAS自我報告嗅覺、味覺、腮腺炎和三叉神經感覺:該問卷主觀測量嗅覺、味覺和三叉神經功能。受試者將在一個包含100個單元的VAS係統上填寫一份簡短的問卷,其中的問題與他們目前的嗅覺、味覺和感知三叉神經的能力有關。1康複被認為是至少80%的疾病前功能的改善。
QoD:為了評估嗅覺特定的生活質量,將使用英文驗證版本的翻譯QoD。對於前24個問題,答案按四個選項排序:同意、部分同意、部分不同意、不同意。其中兩個問題需要回答是或否,另外九個問題采用李克特10分製。29 30
統計分析
所有統計分析將使用IBM SPSS Statistics V.27.0軟件和R統計計算進行。將使用正態性檢驗來評估變量是否正態分布。我們希望減少丟失的數據。如果滿足多重imputation的假設,可能缺失的數據將用多重imputation處理。分析將在意向治療的基礎上進行。
主要研究參數:主要研究參數是兩組(強的鬆龍或安慰劑)治療後SST的TDI評分差異。TDI評分5.5的差異被確定為與主要結局的臨床相關差異。34平均值(或中位數)和標準差(或範圍)將被報告。根據結果的分布,我們將使用非配對t檢驗或Mann-Whitney U檢驗來確定幹預組和對照組之間的統計差異。
二次研究參數:用TST方法評估目標味覺功能,評估四種基本味覺的識別閾值和識別得分範圍為0-16。32臨床改善定為>2分。35TST得分和不同問卷的得分分別在開始時和開始後12周進行測量。平均值(或中位數)和標準差(或範圍)將被報告。根據結果的分布,我們將使用非配對t檢驗或Mann-Whitney U檢驗來確定幹預組和對照組之間的統計差異。
道德和傳播
UMCU的機構審查委員會批準了研究方案(方案編號:21-635/G-D, 2021年10月)。這項研究將根據《赫爾辛基宣言》的原則進行(2013年,福塔萊薩),並根據《涉及人體受試者的醫學研究法》、《歐洲聯盟一般數據保護條例》以及其他準則、條例和法案,例如《gebruik法典》。對於本方案,使用了《標準方案項目:介入試驗建議清單》。試驗報告綜合標準將用於完整的隨機對照試驗報告。
所有實質性的修訂將通知醫學倫理委員會和主管當局。數據處理和保護是根據ISO標準(27001和9001)、國際良好臨床實踐協調會議(ICH-GCP)和適用的法規進行的。我們將始終保持保密,參與者的信息不會泄露給第三方。隻有直接參與這項研究的研究人員才能訪問所有收集到的研究數據。患者將收到一個唯一的標識符,之後,研究團隊的成員將提取所有必要的臨床參數到eCRF Castor EDC和IBM SPSS Statistics V.27.0中,這是由密碼保護的,位於一個鎖上的房間。一個本地監控器(UMCU)將監控試驗質量。不良事件(AEs)將記錄在Castor EDC中,嚴重的AEs將報告給主辦方。讚助商將通過門戶報告saeToetsingOnline經認證的醫學倫理委員會批準了該議定書
倫理語句
病人同意發表
參考文獻
腳注
貢獻者ejas -手稿作者和執行調查員。dmark - COCOS研究的原稿作者、首席研究員、耳鼻咽喉科主任、聯合發起人。IS-epidemiology檢查。sb輸入測試裝置和測試材料。WMB-clinical設置檢查。COCOS研究的rjs啟動者。
資金這項工作得到了荷蘭衛生組織(ZonMW;項目編號:10430102110001)。
相互競爭的利益沒有宣布。
患者和公眾的參與患者和/或公眾參與了本研究的設計、實施、報告或傳播計劃。有關更多細節,請參閱方法部分。
來源和同行評審不是委托;外部同行評議。


